HIDROKARBON
 Dalam bidang kimia, hidrokarbon adalah sebuah senyawa yang terdiri dari unsur atom karbon (C) dan atom hidrogen
(H). Seluruh hidrokarbon memiliki rantai karbon dan atom-atom hidrogen
yang berikatan dengan rantai tersebut. Istilah tersebut digunakan juga
sebagai pengertian dari hidrokarbon alifatik.
Dalam bidang kimia, hidrokarbon adalah sebuah senyawa yang terdiri dari unsur atom karbon (C) dan atom hidrogen
(H). Seluruh hidrokarbon memiliki rantai karbon dan atom-atom hidrogen
yang berikatan dengan rantai tersebut. Istilah tersebut digunakan juga
sebagai pengertian dari hidrokarbon alifatik.
Sebagai contoh, metana (gas rawa) adalah hidrokarbon dengan satu atom karbon dan empat atom hidrogen: CH4. Etana
adalah hidrokarbon (lebih terperinci, sebuah alkana) yang terdiri dari
dua atom karbon bersatu dengan sebuah ikatan tunggal, masing-masing
mengikat tiga atom karbon: C2H6. Propana memiliki tiga atom C (C3H8) dan seterusnya (CnH2·n+2)
Klasifikasi Hidrokarbon
Klasifikasi hidrokarbon yang dikelompokkan oleh tatanama organik adalah:
- Hidrokarbon jenuh/tersaturasi (alkana) adalah hidrokarbon yang paling sederhana. Hidrokarbon ini seluruhnya terdiri dari ikatan tunggal dan terikat dengan hidrogen. Rumus umum untuk hidrokarbon tersaturasi adalah CnH2n+2.Hidrokarbon jenuh merupakan komposisi utama pada bahan bakar fosil dan ditemukan dalam bentuk rantai lurus maupun bercabang. Hidrokarbon dengan rumus molekul sama tapi rumus strukturnya berbeda dinamakan isomer struktur.
- Hidrokarbon tak jenuh/tak tersaturasi adalah hidrokarbon yang memiliki satu atau lebih ikatan rangkap, baik rangkap dua maupun rangkap tiga. Hidrokarbon yang mempunyai ikatan rangkap dua disebut dengan alkena, dengan rumus umum CnH2n.Hidrokarbon yang mempunyai ikatan rangkap tiga disebut alkuna, dengan rumus umum CnH2n-2.
- Sikloalkana adalah hidrokarbon yang mengandung satu atau lebih cincin karbon. Rumus umum untuk hidrokarbon jenuh dengan 1 cincin adalah CnH2n.
- Hidrokarbon aromatik, juga dikenal dengan arena, adalah hidrokarbon yang paling tidak mempunyai satu cincin aromatik.
Hidrokarbon dapat berbentuk gas (contohnya metana dan propana), cairan (contohnya heksana dan benzena), lilin atau padatan dengan titik didih rendah (contohnya paraffin wax dan naftalena) atau polimer (contohnya polietilena, polipropilena dan polistirena).
Ciri-ciri umum
Karena struktur molekulnya berbeda, maka
rumus empiris antara hidrokarbon pun juga berbeda: jumlah hidrokarbon
yang diikat pada alkena dan alkuna pasti lebih sedikit karena atom
karbonnya berikatan rangkap.
Kemampuan hidrokarbon untuk berikatan dengan dirinya sendiri disebut dengan katenasi, dan menyebabkan hidrokarbon bisa membentuk senyawa-senyawa yang lebih kompleks, seperti sikloheksana atau arena seperti benzena. Kemampuan ini didapat karena karakteristik ikatan diantara atom karbon bersifat non-polar.
Sesuai dengan teori ikatan valensi, atom karbon harus memenuhi aturan “4-hidrogen”
yang menyatakan jumlah atom maksimum yang dapat berikatan dengan
karbon, karena karbon mempunyai 4 elektron valensi. Dilihat dari
elektron valensi ini, maka karbon mempunyai 4 elektron yang bisa
membentuk ikatan kovalen atau ikatan dativ.
Hidrokarbon bersifat hidrofobik dan termasuk dalam lipid.
Beberapa hidrokarbon tersedia melimpah di tata surya. Danau berisi metana dan etana cair telah ditemukan pada Titan, satelit alam terbesar Saturnus, seperti dinyatakan oleh Misi Cassini-Huygens.
Hidrokarbon sederhana dan variasinya
| Jumlah atom karbon |
Alkana(1 ikatan) | Alkena(2 ikatan) | Alkuna (3 ikatan) | Sikloalkana | Alkadiena |
|---|---|---|---|---|---|
| 1 | Metana | Metena | Metuna | – | – |
| 2 | Etana | Etena (etilena) | Etuna (asetilena) | – | – |
| 3 | Propana | Propena (propilena) | Propuna (metilasetilena) | Siklopropana | Propadiena (alena) |
| 4 | Butana | Butena (butilena) | Butuna | Siklobutana | Butadiena |
| 5 | Pentana | Pentena | Pentuna | Siklopentana | Pentadiena (piperylene) |
| 6 | Heksana | Heksena | Heksuna | Sikloheksana | Heksadiena |
| 7 | Heptana | Heptena | Heptuna | Sikloheptana | Heptadiena |
| 8 | Oktana | Oktena | Oktuna | Siklooktana | Oktadiena |
| 9 | Nonana | Nonena | Nonuna | Siklononana | Nonadiena |
| 10 | Dekana | Dekena | Dekuna | Siklodekana | Dekadiena |
Penggunaan
Hidrokarbon adalah salah satu sumber energi paling penting di bumi. Penggunaan yang utama adalah sebagai sumber bahan bakar. Dalam bentuk padat, hidrokarbon adalah salah satu komposisi pembentuk aspal.[6]
Hidrokarbon dulu juga pernah digunakan untuk pembuatan klorofluorokarbon, zat yang digunakan sebagai propelan pada semprotan nyamuk. Saat ini klorofluorokarbon tidak lagi digunakan karena memiliki efek buruk terhadap lapisan ozon.
Metana dan etana berbentuk gas dalam suhu ruangan dan tidak mudah dicairkan dengan tekanan begitu saja. Propana lebih mudah untuk dicairkan, dan biasanya dijual di tabung-tabung dalam bentuk cair. Butana sangat mudah dicairkan, sehingga lebih aman dan sering digunakan untuk pemantik rokok. Pentana berbentuk cairan bening pada suhu ruangan, biasanya digunakan di industri sebagai pelarut wax dan gemuk. Heksana biasanya juga digunakan sebagai pelarut kimia dan termasuk dalam komposisi bensin.
Heksana, heptana, oktana, nonana, dekana, termasuk dengan alkena dan beberapa sikloalkana merupakan komponen penting pada bensin, nafta, bahan bakar jet,
dan pelarut industri. Dengan bertambahnya atom karbon, maka hidrokarbon
yang berbentuk linear akan memiliki sifat viskositas dan titik didih
lebih tinggi, dengan warna lebih gelap.
ALKANA
Alkana (juga disebut dengan parafin) adalah senyawa kimia hidrokarbon jenuh asiklis. Alkana termasuk senyawa alifatik. Dengan kata lain, alkana adalah sebuah rantai karbon panjang dengan ikatan-ikatan tunggal. Rumus umum untuk alkana adalah CnH2n+2. Alkana yang paling sederhana adalah metana dengan rumus CH4. Tidak ada batasan berapa karbon yang dapat terikat bersama. Beberapa jenis minyak dan wax adalah contoh alkana dengan atom jumlah atom karbon yang besar, bisa lebih dari 10 atom karbon.
Setiap atom karbon mempunyai 4 ikatan (baik ikatan C-H atau ikatan C-C),
dan setiap atom hidrogen mesti berikatan dengan atom karbon (ikatan
H-C). Sebuah kumpulan dari atom karbon yang terangkai disebut juga
dengan rumus kerangka. Secara umum, jumlah atom karbon digunakan untuk mengukur berapa besar ukuran alkana tersebut (contohnya: C2-alkana).
Gugus alkil, biasanya disingkat dengan simbol R, adalah gugus fungsional, yang seperti alkana, terdiri dari ikatan karbon tunggal dan atom hidrogen, contohnya adalah metil atau gugus etil.
Klasifikasi struktur
Hidorkarbon tersaturasi dapat berupa:
- lurus (rumus umum CnH2n + 2), kerangka karbon membentuk rantai lurus tanpa ada cabang
- bercabang (rumus umum CnH2n + 2, n > 3), kerangka karbon utamanya mempunyai cabang-cabang
- siklik (rumus umum CnH2n, n > 2), ujung-ujung kerangka karbonnya bertemu sehingga membentuk suatu siklus.
Menurut definisi dari IUPAC, 2 golongan pertama di atas dinamakan alkana, sedangkan golongan yang ketiga disebut dengan sikloalkana.Hidrokarbon
tersaturasi juga dapat membentuk gabungan ketiga macam rantai diatas,
misalnya linear dengan siklik membentuk polisiklik. Senyawa seperti ini
masih disebut dengan alkana (walaupun tidak mempunyai rumus umum),
sepanjang tetap berupa asiklik (tidak seperti siklus).
Keisomeran
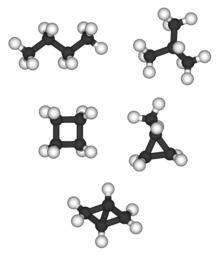
C4-alkana dan -sikloalkana yang berbeda-beda (kiri ke kanan): n-butana dan isobutana adalah 2 isomer C4H10; siklobutana dan metilsiklopropana adalah 2 isomer C4H8.
Bisiklo[1.1.0]butana (C4H6) tidak mempunyai isomer; tetrahedrana (tidak terlihat) (C4H4) juga tidak mempunyai isomer.
Bisiklo[1.1.0]butana (C4H6) tidak mempunyai isomer; tetrahedrana (tidak terlihat) (C4H4) juga tidak mempunyai isomer.
Alkana dengan 3 atom karbon atau lebih dapat disusun dengan banyak macam cara, membentuk isomer struktur yang berbeda-beda. Sebuah isomer, sebagai sebuah bagian, mirip dengan anagram kimia, tapi berbeda dengan anagram, isomer dapat berisi jumlah komponen dan atom yang berbeda-beda, sehingga sebuah senyawa kimia
dapat disusun berbeda-beda strukturnya membentuk kombinasi dan
permutasi yang beraneka ragam. Isomer paling sederhana dari sebuah
alkana adalah ketika atom karbonnya terpasang pada rantai tunggal tanpa
ada cabang. Isomer ini disebut dengan n-isomer (n
untuk “normal”, penulisannya kadang-kadang tidak dibutuhkan). Meskipun
begitu, rantai karbon dapat juga bercabang di banyak letak. Kemungkinan
jumlah isomer akan meningkat tajam ketika jumlah atom karbonnya semakin
besar.Contohnya:
- C1: tidak memiliki isomer: metana
- C2: tidak memiliki isomer: etana
- C3: tidak memiliki isomer: propana
- C4: 2 isomer: n-butana & isobutana
- C5: 3 isomer: pentana, isopentana, neopentana
- C6: 5 isomer: heksana, 2-Metilpentana, 3-Metilpentana, 2,3-Dimetilbutana & 2,2-Dimetilbutana
- C12: 355 isomer
- C32: 27.711.253.769 isomer
- C60: 22.158.734.535.770.411.074.184 isomer, banyak diantaranya tidak stabil.
Tata nama
Tata nama IUPAC untuk alkana didasarkan
dari identifikasi rantai hidrokarbon. Rantai hidrokarbon tersaturasi,
tidak bercabang maka dinamai sistematis dengan akhiran “-ana”.
Rantai karbon lurus
Alkana rantai karbon lurus biasanya dikenalo dengan awalan n- (singkatan dari normal) ketika tidak ada isomer.
Meskipun tidak diwajibkan, tapi penamaan ini penting karena alkana
rantai lurus dan rantai bercabang memiliki sifat yang berbeda. Misalnya n-heksana atau 2- atau 3-metilpentana.
Anggota dari rantai lurus ini adalah:
- Metana, CH4 – 1 karbon dan 4 hidrogen
- Etana, C2H6 – 2 karbon dan 6 hidrogen
- Propana, C3H8 – 3 karbon dan 8 hidrogen
- Butana, C4H10 – 4 karbon dan 10 hidrogen
- pentana, C5H12 – 5 karbon dan 12 hidrogen
- heksana, C6H14 – 6 carbon dan 14 hidrogen
Mulai dengan jumlah karbon mulai dari lima diberi nama dengan imbuhan jumlah yang ditentukan IUPAC diakhiri dengan -ana. Contohnya antara lain adalah pentana, heksana, heptana, dan oktana.
Rantai karbon bercabang
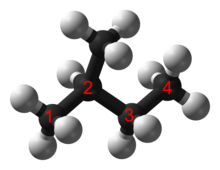
Model dari isopentana (nama umum) atau 2-metilbutana (nama sistematik IUPAC)
Untuk memberi nama alkana dengan rantai bercabang digunakan langkah-langkah berikut:
- Cari rantai atom karbon terpanjang
- Beri nomor pada rantai tersebut, dimulai dari ujung yang terdekat dengan cabang
- Beri nama pada cabang-cabangnya
Nama alkana dimulai dengan nomor letak cabang, nama cabang, dan nama rantai utama. Contohnya adalah 2,2,4-trimetilpentana yang disebut juga isooktana. Rantai terpanjangnya adalah pentana, dengan tiga buah cabang metil (trimetil) pada karbon nomor 2, 2, dan 4.
| Nama umum/trivial | n-pentana | isopentana | neopentana |
|---|---|---|---|
| Nama IUPAC | pentana | 2-metilbutana | 2,2-dimetilpentana |
| Struktur |  |
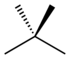 |
Alkana siklik
Sikloalkana adalah hidrokarbon yang seperti alkana, tapi rantai karbonnya membentuk cincin.
Sikloalkana sederhana mempunyai awalan
“siklo-” untuk membendakannya dari alkana. Penamaan sikloalkana dilihat
dari berapa banyak atom karbon yang dikandungnya, misalnya siklopentana (C5H10) adalah sikloalkana dengan 5 atom karbon seperti pentana(C5H12), hanya saja pada siklopentana kelima atom karbonnya membentuk cincin. Hal yang sama berlaku untuk propana dan siklopropana, butana dan siklobutana, dll.
Sikloalkana substitusi dinamai mirip
dengan alkana substitusi – cincin sikloalkananya tetap ada, dan
substituennya dinamai sesuai dengan posisi mereka pada cincin tersebut,
pemberian nomornya mengikuti aturan Cahn-Ingold-Prelog.[3]
Nama-nama trivial
Nama trivial (non-IUPAC) dari alkana adalah “parafin.”
Nama trivial dari senyawa-senyawa ini biasanya diambil dari
artefak-artefak sejarah. Nama trivial digunakan sebelum ada nama
sistematik, dan sampai saat ini masih digunakan karena penggunaannya
familier di industri.
Dapat hampir dipastikan kalau nama parafin diambil dari industri petrokimia. Alkana rantai bercabang disebut isoparafin. Penggunaan kata “paraffin” untuk sebutan secara umum dan seringkali tidak membedakan antara senyawa murni dan campuran isomer dengan rumus kimia yang sama.
Beberapa nama ini dipertahankan oleh IUPAC
- Isobutana untuk 2-metilpropana
- Isopentana untuk 2-metilbutana
- Isooktana untuk 2,2,4-trimetilpentana
- Neopentana untuk 2,2-dimetilpropana
Ciri-ciri fisik
Tabel alkana
| Alkana | Rumus | Titik didih [°C] | Titik lebur [°C] | Massa jenis [g·cm3] (20°C) |
| Metana | CH4 | -162 | -183 | gas |
| Etana | C2H6 | -89 | -172 | gas |
| Propana | C3H8 | -42 | -188 | gas |
| Butana | C4H10 | 0 | -138 | gas |
| Pentana | C5H12 | 36 | -130 | 0.626 (cairan) |
| Heksana | C6H14 | 69 | -95 | 0.659 (cairan) |
| Heptana | C7H16 | 98 | -91 | 0.684 (cairan) |
| Oktana | C8H18 | 126 | -57 | 0.703 (cairan) |
| Nonana | C9H20 | 151 | -54 | 0.718 (cairan) |
| Dekana | C10H22 | 174 | -30 | 0.730 (cairan) |
| Undekana | C11H24 | 196 | -26 | 0.740 (cairan) |
| Dodekana | C12H26 | 216 | -10 | 0.749 (cairan) |
| Ikosana | C20H42 | 343 | 37 | padat |
| Triakontana | C30H62 | 450 | 66 | padat |
| Tetrakontana | C40H82 | 525 | 82 | padat |
| Pentakontana | C50H102 | 575 | 91 | padat |
| Heksakontana | C60H122 | 625 | 100 | padat |
ALKENA
Alkena atau olefin dalam kimia organik adalah hidrokarbon tak jenuh dengan sebuah ikatan rangkap dua antara atom karbon. Alkena asiklik yang paling sederhana, yang membentuk satu ikatan rangkap dan tidak berikatan dengan gugus fungsional manapun, maka akan membentuk suatu kelompok hidrokarbon dengan rumus umum CnH2n.
Alkena yang paling sederhana adalah etena atau etilena (C2H4) Senyawa aromatik
seringkali juga digambarkan seperti alkena siklik, tapi struktur dan
ciri-ciri mereka berbeda sehingga tidak dianggap sebagai alkena
Tatanama IUPAC
Untuk mengikuti tatanama IUPAC, maka seluruh alkena memiliki nama yang diakhiri -ena. Pada dasarnya, nama alkena diambil dari nama alkana dengan menggantikan akhiran -ana dengan -ena. C2H6 adalah alkana bernama etana sehingga C2H4 diberi nama etena.
Pada alkena yang memiliki kemungkinan
ikatan rangkap di beberapa tempat, digunakan penomoran dimulai dari
ujung yang terdekat dengan ikatan tersebut sehingga atom karbon pada
ikatan rangkap bernomor sekecil mungkin untuk membedakan isomernya. Contohnya adalah 1-heksena dan 2-heksena. Penamaan cabang sama dengan alkana.
Pada alkena yang lebih tinggi, dimana terdapat isomer yang letaknya berbeda dengan letak ikatan rangkap, maka sistem penomoran berikut ini dipakai:
- Penomoran rantai karbon terpanjang dilihat dari ujung yang terdekat dengan ikatan rangkap, sehingga atom karbon pada ikatan rangkap tersebut mempunyai nomor sekecil mungkin.
- Ketahui letak ikatan rangkap dengan letak karbon rangkap pertamanya.
- Penamaan rantai alkena itu mirip dengan alkana.
- Beri nomor pada atom karbon, ketahui letak lokasi dan nama gugusnya, ketahui letak ikatan rangkap, lalu terakhir namai rantai utamanya.

Berbagai contoh penamaan isomer
1-heksena. Gambar kiri: 1-heksena, gambar tengah: 4-metil-1-heksena,
gambar kanan: 4-etil-2-metil-1-heksena.
Notasi Cis-Trans
Dalam sebuah kasus khusus pada alkena dimana 2 atom karbon mempunyai 2 gugus yang sejenis, maka notasi cis-trans dapat dipakai. Jika gugus sejenis terletak pada tempat yang sama dari ikatan rangkap, maka disebut sebagai (cis-). Jika gugus sejenis terletak berseberangan, maka disebut sebagai (trans-).ALKUNA
Alkuna adalah hidrokarbon tak jenuh yang memiliki ikatan rangkap tiga. Secara umum, rumus kimianya CnH2n-2. Salah satunya adalah etuna yang disebut juga sebagai asetilen dalam perdagangan atau sebagai pengelasan.
Tata Nama
Semua anggota alkuna berakhiran -una dan menurut IUPAC.
Rantai karbon lurus
Untuk alkuna rantai lurus, dinamakan sesuai dengan alkana dengan jumlah atom karbon yang sama, namun diakhiri dengan -una. Berikut adalah alkuna dengan jumlah atom karbon 2-10 disebut:
- Etuna, C2H2
- Propuna, C3H4
- Butuna, C4H6
- Pentuna, C5H8
- Heksuna, C6H10
- Heptuna, C7H12
- Oktuna, C8H14
- Nonuna, C9H16
- Dekuna, C10H18
Rantai karbon bercabang
Untuk memberikan nama alkuna dengan
rantai bercabang sama mirip dengan alkana rantai bercabang. Namun
“rantai utama” pada proses penamaan haruslah melalui ikatan rangkap 3,
dan prioritas penomoran dimulai dari ujung yang terdekat ke ikatan
rangkap 3.














